オートファジーとは
オートファジーは、
自食とも呼ばれる細胞が持っている、細胞内のタンパク質を分解するための仕組みの一つです。
酵母からヒトにいたるまでの真核生物に見られる機構であり、細胞内での異常なタンパク質の蓄積を防いだり、過剰にタンパク質合成したときや栄養環境が悪化したときにタンパク質のリサイクルを行ったり、
細胞質内に侵入した病原微生物を排除することで生体の恒常性維持に関与している。
このほか、個体発生の過程でのプログラム細胞死や、ハンチントン病などの疾患の発生、
細胞のがん化抑制にも関与することが知られている。
auto-はギリシャ語の「自分自身」を表す接頭語、phagyは「食べること」の意。
オートファジーは、そのメカニズムの違いから
(1)マクロオートファジー、(2)ミクロオートファジー、(3)シャペロン介在性オートファジーの3つに分けられます。
マクロオートファジー:細胞がある種のストレス(アミノ酸飢餓の状態や、異常タンパク質の蓄積)に晒(さら)されると、細胞質中の一部で、過剰に作られたタンパク質や異常タンパク質と共にリン脂質が集まり、
オートファゴソーム(Autophagosome、または
オートファジー小胞 Autophagic vesicle)と呼ばれる細胞内構造の形成がはじまります。
オートファジーの役割は、飢餓状態を生き抜くために自己消化することで栄養源を確保していると一般には理解されています。
しかしながら近年では通常の環境下でも
プロテアソーム系と並んで細胞成分の代謝に働いていることがわかっています。
集積したリン脂質は脂質二重膜を形成し、さらにそれが成長していくことで、細胞質成分やオルガネラ(細胞小器官)などを二重のリン脂質の膜で取り囲んだ小胞が形成されます。
この小胞形成には、
Atg(autophagy-deficient mutants)タンパク質と呼ばれる一群のタンパク質が関与しています。
酵母や植物細胞では、形成されたオートファゴソームは液胞と膜融合し、その内部に取り込まれた異物などは液胞内部の分解酵素によって分解されます。
動物細胞においては、オートファゴソームが形成されると、次にオートファゴソームと細胞内のリソソームが膜融合を起こします。
こうしてリソソームと融合したものをオートリソソームと呼びます。
オートリソソームの内部で、オートファゴソームに由来する分解すべきタンパク質と、リソソームに由来するさまざまなタンパク分解酵素が反応し、この結果、オートファゴソームに取り込まれていたタンパク質はアミノ酸やペプチドに分解されます。
このとき、オートファゴソームの二重膜のうち、内側の脂質膜も同時に分解されます。
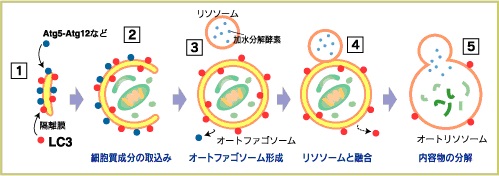
自己消化で得られたアミノ酸は栄養源として再利用されます。
「オートファゴソーム」は、 小胞体とミトコンドリアの接触部から作られる
Atg14は普段は小胞体膜に一様に分布しているが、オートファジーが誘導されると一点に集合し、そこを起点にオートファーゴソームが作られはじめます。
Atg5は隔離膜に結合し、末端が閉じると膜から離脱します。
小胞体とミトコンドリアの接触部位にAtg5のドットがあらわれ、だんだんと大きくなり、最後に消えてなくなります。
オートファゴソームが多数作られる際には、接触部位が両オルガネラの結合膜として分画され、接触部位の隙間にはAtg14というタンパク質が高密度に存在します。
飢餓信号により、小胞体に存在する特定のタンパク質(stx17)がAtg14と結合して、小胞体とミトコンドリアの接触部位へ移動。
移動したAtg14が、膜成分を作るための酵素などを活性化させ、オートファーゴソームを完成させます。
シャペロン介在性オートファジー:シャペロンが異常タンパク質に結合することによって、液胞やリソソームへの取り込みを行い、その内部で分解する機構です。
また分解する対象によって、別の呼び方がされる場合もあります。
ペキソファジー:ペルオキシソームを選択的に分解する。
マイトファジー:ミトコンドリアを選択的に分解する。
ゼノファジー:細胞内に侵入した細菌を分解する。
タンパク質分解との関係
細胞は、タンパク質を新たに作り出す機構だけでなく、作ったタンパク質が不要になった場合に分解する機構も持っています。
この機構をタンパク質分解と呼びますが、これには、
ユビキチン-プロテアソーム系とオートファジーの二つの主要な機構が存在します。
ユビキチン-プロテアソーム系では、分解するべきタンパク質の一つ一つに、
ユビキチン分子が複数結合することでプロテアソームにより認識されて分解されるというかたちで個々のタンパク質ごとの分解が行われるのに対し、オートファジーでは、一度に多くのタンパク質が分解されます。
このため
オートファジーによるタンパク質分解のことはバルク分解とも呼ばれます。
しかし最近では、選ばれたタンパク質や細胞小器官だけが分解されるという選択的オートファジーの存在が明らかになってきました。
栄養飢餓
細胞が生命活動を行うためには、必要な遺伝子を発現させて、タンパク質などの生体高分子を生合成する必要があります。
タンパク質はアミノ酸からなる高分子であり、細胞が生命活動を行うためにはその材料となる必須アミノ酸を、栄養源として細胞外から取り込む必要があります。
個体が飢餓状態におかれて栄養が枯渇し、アミノ酸の供給が断たれることは、細胞にとっては生死に関わる重大なダメージになります。
しかしオートファジーが働くことによって、細胞は一時的にこのダメージを回避することが可能だと考えられています。
オートファジーが起きると、細胞内に常に存在しているタンパク質(ハウスキーピング蛋白)の一部が分解されて、ペプチドやアミノ酸が生成され、それが細胞の生命活動にとって、より重要性の高いタンパク質を合成する材料に充てられると考えられています。
この機構は動物の個体レベルにおいても観察され、例えばマウスを一晩絶食させることで、肝細胞でオートファジーが起きることが知られています。
ただし、オートファジーによる栄養飢餓の回避はあくまで一時的なものであり、飢餓状態が長く続いた場合には対処することができません。
この場合、オートファジーが過度に進行することで、細胞が自分自身を「食べ尽くし」てしまい、細胞が死に至ると考えられてます。
感染防御
オートファジーの機構とよく似たものの一つに、マクロファージや好中球などの食細胞が行う貪食(どんしょく、ファゴサイトーシス)があります。
これらの食細胞は、体内に侵入した異物や病原体をエンドサイトーシスによって、ファゴソームという小胞に包んだ形で取り込みます。
ファゴソームは細胞質内で、オートファゴソームと同様にリソソームと膜融合してファゴリソソームとなり小胞内部の異物を消化分解します。
しかしリステリア属の細菌は、内部からファゴソームを破壊して貪食の機構から逃れ、細胞質内に感染(細胞内感染)しようとする。オートファジーはこのようにして細胞質内に逃れた細菌を、再び捕えなおして分解する働きも果たしており、この働きによって生体を微生物による感染から守っていると考えられています。
細胞死の種類とメカニズム
オンコーシス(ネクローシス)は細胞の集団死

