親電子性物質とは
遺伝子が壊れる要因には、X線や紫外線などがありますが、その中の一つに親電子性物質というもの(他の物質にくっつくと電子を奪う)があります。
親電子性物質は天然の食べ物を摂取することでも普通に出てくるもので、ゼロにすることは不可能です。
動物は基本的に、植物が光合成で作った糖分を奪い、酸素を使ってそれを燃やして、エネルギーを生産しています。
一方、植物のほうは単純に食べられてくれるわけではありません。
植物は捕食者である動物に化学戦(chemical war) を挑む目的で、毒性のある産物を産生します。
また、私たちの
体は酸素の毒性・酸化ストレスを受けて錆びていくこともよく知られています。
このような
環境からのストレスの存在にもかかわらず、私たちが生きていくことができるのは、私たちの体に、そのような
食物由来毒物や酸素が内包するストレスを感知して、それに応答する生体防御遺伝子の発現を誘導するようなメカニズムをもっている為です。
また、環境の中には、化学発癌物質も沢山あり、これらの
化学発癌物質も親電子性の強い分子です。
内部に電子が少ない部分をもった分子のことを親電子性物質(electrophiles) と呼びますが、DNAやタンパク質のような生体高分子は、電子を与える性質に溢れているので、
親電子性物質はそれらと共有結合を作り、ある時には発癌、ある時には
急性毒性を惹起(じゃっき)します。
環境中の
ベンゾピレンや
アフラトキシンなどは
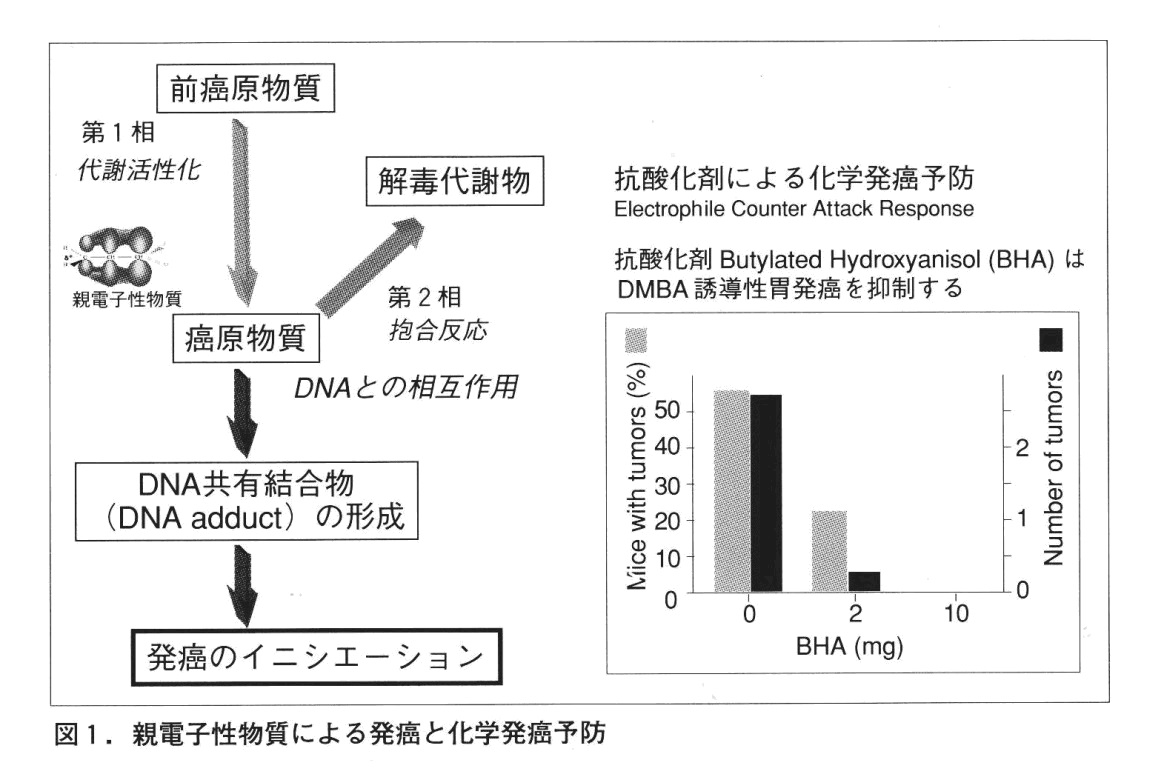
「前癌原物質」であり、これらは体内に取り込まれた後で第1相解毒酵素による代謝活性化を受け、親電子性物質となって初めて、
「癌原物質(発癌物質)」になると考えられています。
通常、これらの
親電子性代謝物はすぐ、第2相解毒酵素群によりグルタチオンやグルクロン酸抱合を受けて、水溶性解毒代謝物になり、体外に容易に排泄されます。
したがって、たとえ前癌原物質を多少摂取しても、私たちの体は簡単には癌にならないのです。
しかし、何かの加減で第2相反応が障害される、もしくは、
癌原物質の量が第2相解毒酵素群の能力をオーバーフローしてしまうと、親電子性物質はDNA共有結合物を作り、発癌のイニシェーションに働きます。(図1)
転写因子Nrf2 は、
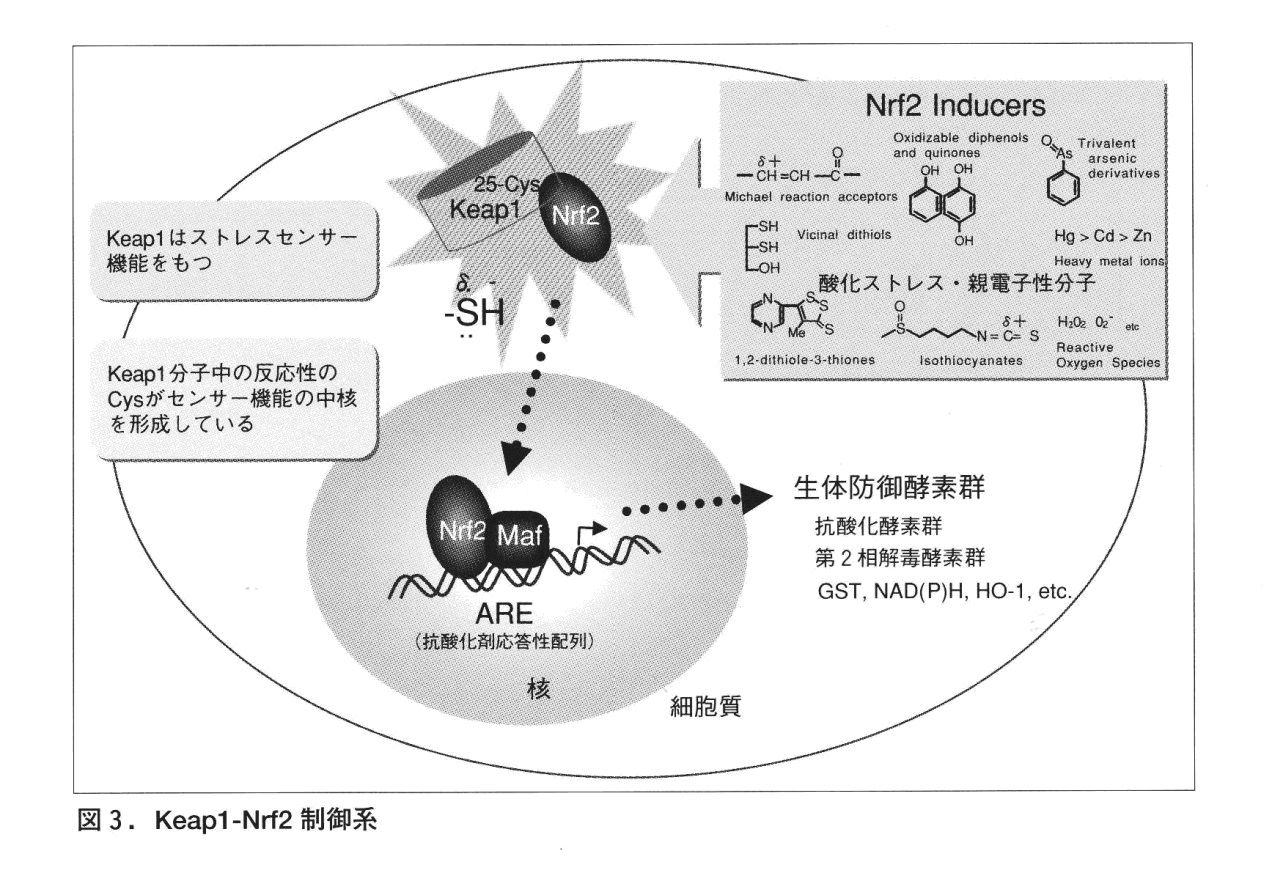
環境中の異物・毒物や酸化ストレスに応答して、一群の生体防御系酵素の誘導発現を行い、生体を環境ストレスから守っています。
また、
Keap1遺伝子はこれらの環境ストレスに対する生体センサーとして働きます。
生体が発癌性毒物に暴露されると、Keap1 がそれを感知し、Nrf2 活性化を誘導して、第2 相解毒酵素群や抗酸化酵素群の発現を誘導する。その結果、発癌物質は解毒され、生体は発癌の危機から逃れる。
一方、癌細胞は往々にしてNrf2-Keap1 系に体細胞性突然変異を蓄積し、強いNrf2 活性を獲得して、自らの増殖に活用している。
Nrf2は、酸化ストレス応答系による病態の制御をします。
転写因子Nrf2は、親電子性物質、活性酸素、小胞体ストレスや
血流によるずり応力によって活性化され、
ヒトにおける酸化ストレス適応反応を統一的に制御します。
毒性学では、
少量のストレスが細胞の防御機構を誘導し引き続く重篤なストレスに耐性となる現象を“ホルミシス”と呼びますが、Nrf2は酸化ストレスに対するホルミシスを仲介すると考えられます。
近年、
ファイトケミカル(健康に良い影響を与えるかもしれない植物由来の化合物)等によるNrf2の活性化が、様々な疾患の予防・治療に有効であることが動物モデルで明らかになりつつあります。(ブロッコリースプラウトに含まれるスルフォラファンには強烈なNrf2の誘導作用があります)
Nrf2は,親電子性物質の解毒化酵素であるグルタチオンS -転移酵素(GST)やNAD(P)H キノン還元酵素(NQO1)などの異物代謝酵素群、グルタチオン合成酵素やヘムオキシゲナゼ1(HO-1)などの酸化ストレス防御遺伝子群、抗炎症性遺伝子群、ユビキチンプロテアソーム系に関与する遺伝子群、ヘム・鉄代謝遺伝子、薬物トランスポーター遺伝子などを統一的に誘導し、ストレスに対する恒常性維持機構として働いています。
Nrf2の活性化機構
非ストレス状態の細胞においてNrf2はKeap1に捕捉されプロテアソームによって分解されます。
細胞が親電子性物質、活性酸素、小胞体ストレスや血管ずり応力の刺激を受けると、Nrf2はKeap1の抑制から開放されて活性化されます。
Keap1は、細胞質に存在し、ストレスセンサーとして働き、Nrf2分解に働く酵素です。
癌細胞はNrf2経路をハイジャック薬剤耐性を獲得
ヒトの肺癌細胞を調べると高度にKeap1遺伝子の変異が存在します。
この突然変異はNrf2を活性化する変異です。
このKeap1変異をもつことによって、癌細胞は周りに対する抵抗性、さらには抗癌剤に対する抵抗性を獲得したものと思われます。
この事は、
多剤耐性・抗癌剤耐性のメカニズムは抗癌剤のABCトランスポーターによる汲み出しである。
すなわち
Nrf2は抗癌剤の排出を制御していること考えられる。
まとめると、結局Nrf2は両刃の剣であり、
癌細胞はNrf2経路をハイジャックし、解毒代謝系と多剤耐性ポンプを誘導して、自らの増殖を助けている。
酸化ストレス・センサータンパク質の分解機構を解明 2012年8月7日
(タンパク質分解による恒常性の維持)
東北大学大学院医学系研究科医化学分野の山本雅之教授らは、公益財団法人東京都医学総合研究所の小松雅明副参事研究員の研究グループとともに、
活性酸素種や毒物などのセンサーであるKeap1 がオートファジー機構により分解されていることを発見しました。
今回の成果は、生体のストレス応答を担うKeap1-Nrf2制御システムの主要因子であるKeap1 とNrf2 が、それぞれプロテアソーム系とオートファジー系という異なるメカニズムによる分解を受けていることを示すものであり、
ストレス応答系の分子メカニズムを理解する上で重要な発見です。
本研究成果は、米国の学術誌Proceedings of the National Academy of Sciences of the United States of America (PNAS)に掲載されました。
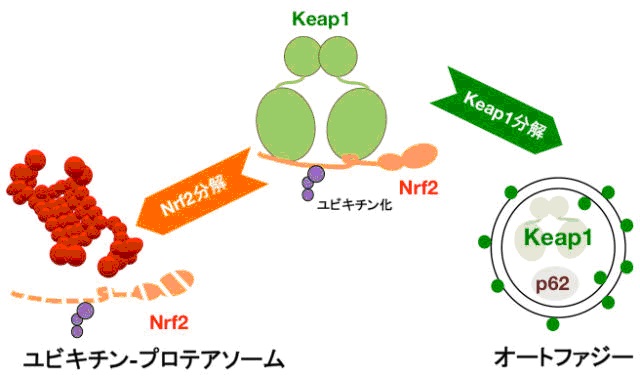 プロテアソームとオートファジーは重要なタンパク質分解機構です。
プロテアソームとオートファジーは重要なタンパク質分解機構です。
Keap1-Nrf2 制御システムは、生体のストレス応答機構の中心的役割を果たしています。
転写因子Nrf2 は様々な生体防御系遺伝子群の発現を活性化して、細胞のストレス応答能を増強します。
一方、Keap1 はプロテアソーム系によるNrf2 分解を促進し、Nrf2 の機能を抑制しています。
細胞に活性酸素種や毒物などのストレスが加わると、Nrf2 の分解が停止します。
これによりNrf2 が機能できるようになり、細胞のストレスに対する抵抗性が高まります。
このように、Nrf2 の機能がタンパク質分解機構と連関して制御されていることが知られていました。
それに対して、Keap1 機能の制御に何らかのタンパク質分解メカニズムが関与しているのかどうかは不明でした。
本研究グループは、オートファジー全体が障害されているAtg7 遺伝子の欠失マウスや選択的オートファジーに必要なp62 タンパク質*4を欠失したマウスを解析することにより、Keap1 がオートファジーにより選択的に分解されることを明らかにしました。
この成果は、ストレス応答を担うセンサー分子Keap1 と転写因子Nrf2 が、それぞれ異なる経路により分解されていることを示すものであり、多様なタンパク質分解経路により生体のストレス応答が精巧に制御されていることを実証する重要な発見です。
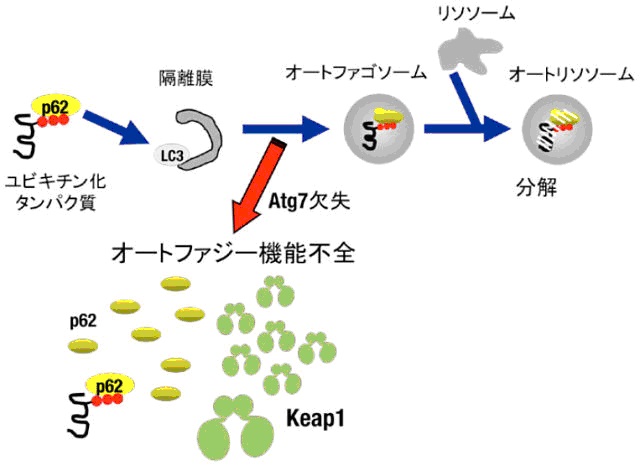
図のように、オートファジー機能不全によるKeap1 およびp62 の蓄積オートファゴソーム形成に必須のAtg7 遺伝子の欠失によりオートファジーの機能を破綻させたマウスにおいては、p62 と同様にKeap1 がタンパク質レベルで蓄積した。
がん細胞の悪性化をもたらす代謝の制御機構を発見
米国学術誌Cancer Cell 22, 1-14, July 10, 2012.に掲載されました。
国立がん研究センター研究所 がんゲノミクス研究分野の柴田龍弘分野長らは、がん細胞の悪性化をもたらす新たな代謝制御機構を発見しました。
正常細胞の中で
酸化ストレス応答を担うタンパク質Nrf2 が、がん細胞の中では糖・アミノ酸代謝を変化させることにより、がん細胞の増殖を促進することを突き止めました。
この結果は、がん細胞の悪性化過程を理解する上で重要な発見です。
本研究成果は、東北大学大学院医学系研究科ラジオアイソトープセンターの本橋ほづみ准教授、同医化学分野の光石陽一郎博士、田口恵子助教、山本雅之教授、東京大学先端科学技術研究センターの油谷浩幸教授との共同研究によるものです。
論文タイトル
「転写因子Nrf2 はグルコースとグルタミンの代謝を改変して同化反応を促進する」
転写因子Nrf2 が非小細胞性肺がんで高頻度に
活性化型変異を起こしていることを報告し、またNrf2 が強く発現している肺がん症例では、予後が極めて不良であることが両機関を含め複数の施設から報告され、
肺がんの悪性化を担っているタンパク質の一つが、Nrf2 であることが解明されてきました。
また、肺がん以外でも
食道がんや胆のうがんなどで、Nrf2が異常に安定化して核内に蓄積している症例がみつかっています。
Nrf2 は、本来、酸化ストレス応答や異物代謝などの生体防御機構で中心的な役割を果たしている転写因子です(図1)
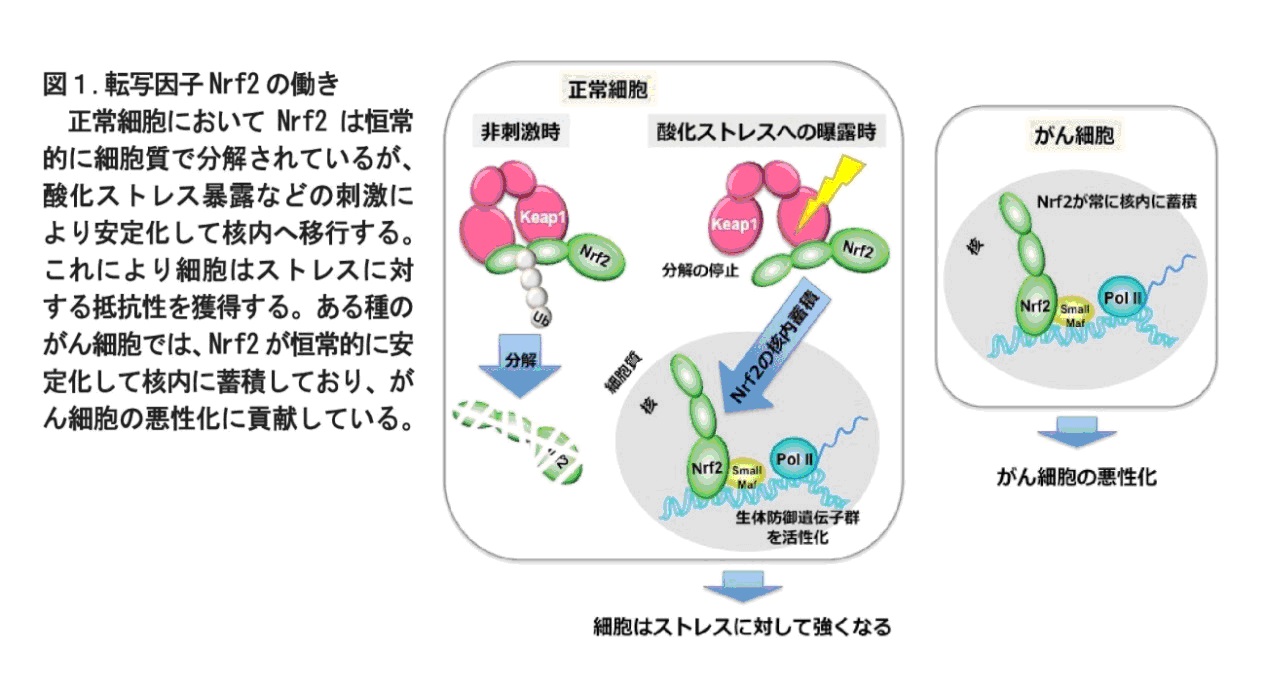
通常の状態では、Nrf2 は細胞質で常に分解されており、その存在はほとんど検出できませんが、
細胞が酸化ストレスや毒物に曝露されると、Nrf2 は安定化して核内に蓄積し、DNA に結合して生体防御に重要な遺伝子群を活性化します。
その結果、抗酸化タンパク質や解毒酵素が誘導されて、細胞の障害は最小限にとどめられます。
したがって、
Nrf2 ががん細胞で恒常的に安定化すると、生体防御遺伝子群が常に活性化され、その結果、がん細胞は抗がん剤や放射線照射に対する抵抗性を獲得し、治療が困難になると理解されてきました。
しかし、
Nrf2 が高発現しているがん細胞では、細胞増殖そのものが亢進していることが観察されており、その理由は不明でした。
今回の発見
活発に増殖するがん細胞では,細胞を構成するさまざまな物質の生合成がさかんであり、グルコースやグルタミンなどの栄養分が大量に消費されています。
さまざまながん遺伝子の活性化もしくは、がん抑制遺伝子の機能喪失により、細胞内の代謝が改変され(代謝リプログラミング)、がん細胞では細胞の増殖に有利な代謝様式が実現しています。
Nrf2 が肺がん細胞において活性化する遺伝子を網羅的に調べたところ、
グルコースの代謝、グルタミンの代謝に関与する酵素群の遺伝子が直接Nrf2 により活性化されることがわかりました。
グルコースの代謝経路のうち、ペントースリン酸経路を触媒する主な4つの酵素がNrf2 の標的遺伝子となっていました。
グルタミンの代謝経路のうち、これまで知られていたグルタチオン合成に関わる酵素に加えて、グルタミンから乳酸を生成する経路の酵素もNrf2 により直接制御されていることもわかりました。
肺がん細胞においてNrf2 が代謝の流れにどのような影響を与えているかを調べると、
Nrf2 は核酸合成とグルタチオン合成を強力に促進することがわかりました。
これらはいずれも細胞の増殖にとって有利な
同化反応です。
すなわち、
Nrf2 の活性化はグルコースを核酸合成へ、グルタミンをグルタチオン合成へと向かわせることで、細胞増殖に有利な代謝を実現していることがわかりました(図2)。
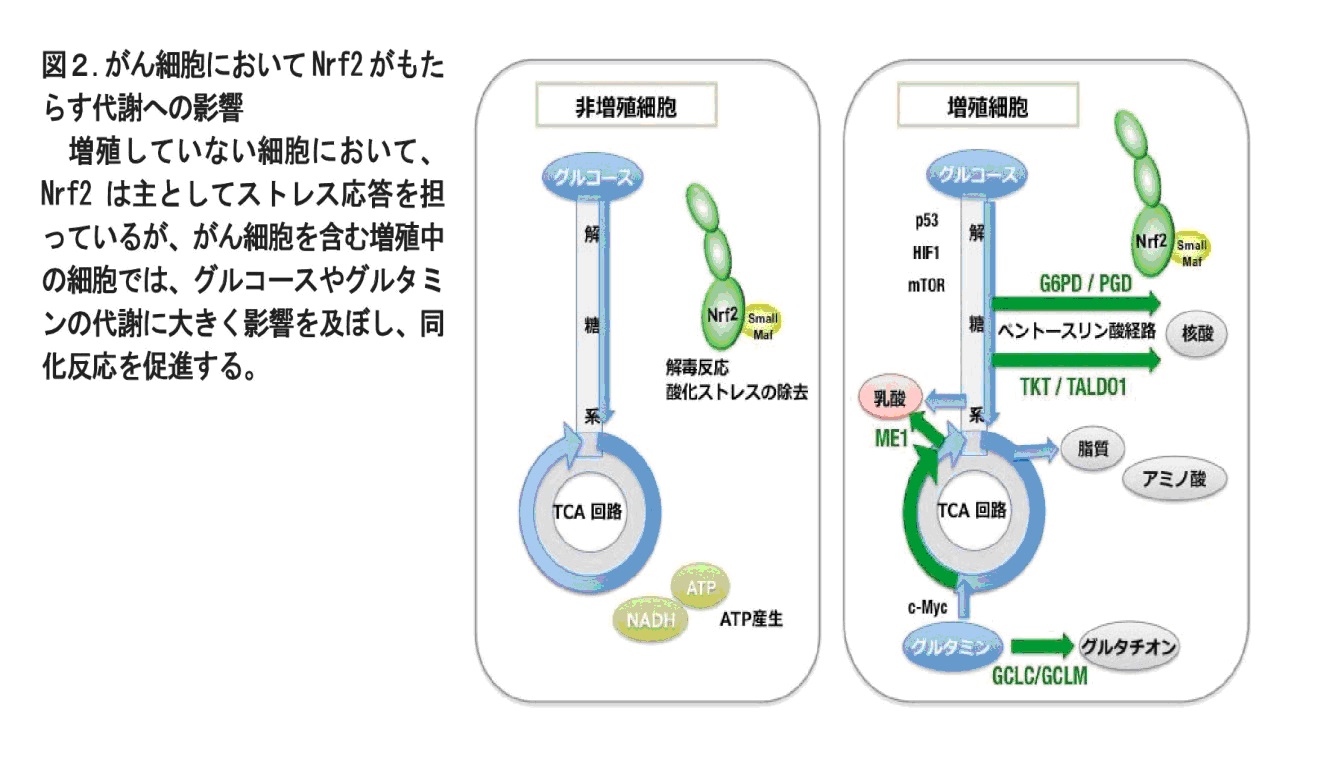
こうしたNrf2 の代謝への影響は、増殖が盛んな細胞において特に強く認められることがわかりました。
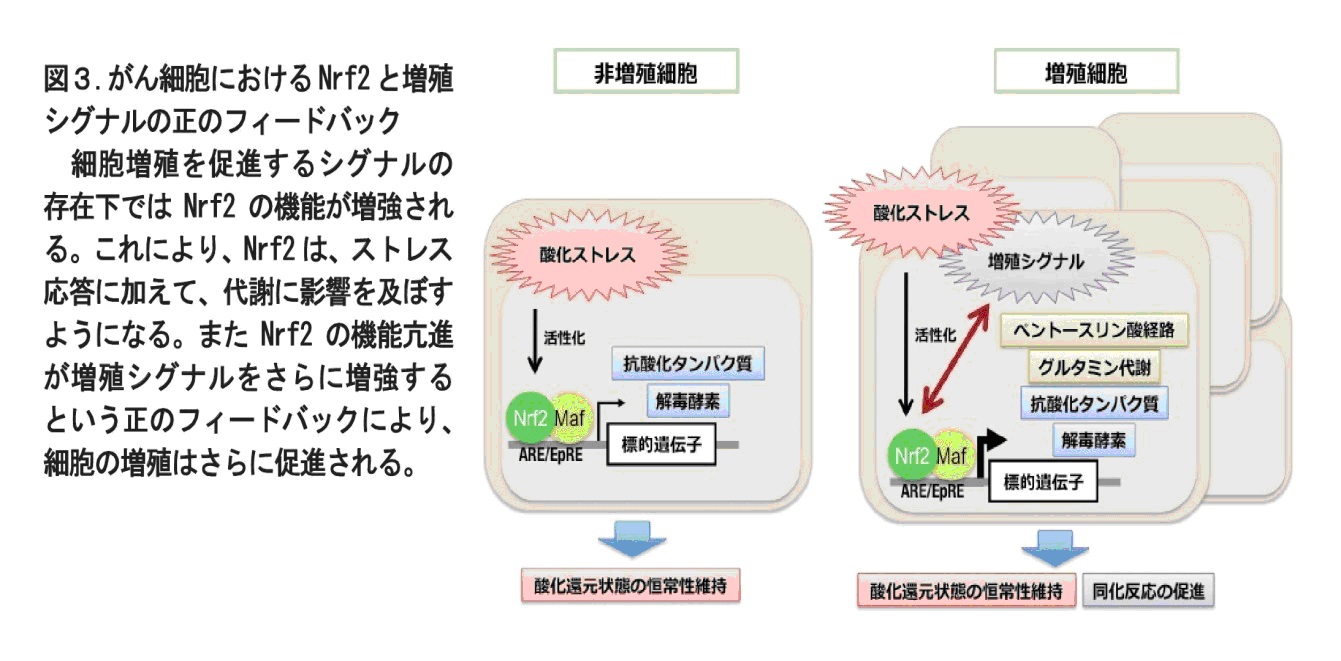
増殖していない細胞では、Nrf2 は主として酸化ストレス応答、解毒代謝機能を担っていますが、増殖を促進する刺激が細胞に作用するとNrf2 の機能が強まり、その結果、Nrf2 はグルコースやグルタミンの代謝の流れを改変する作用を発揮できるようになることがわかりました。
さらに、Nrf2 機能の亢進は増殖シグナルの増幅も誘導し、Nrf2 機能と増殖シグナルとの間の正のフィードバック機構が細胞増殖をさらに促進していると考えられました(図3)。
 意義
意義
20 世紀初頭にオットー・ワールブルグは、がん細胞が正常の細胞とは異なる特徴的な代謝様式を用いていることを発見し、その代謝様式はワールブルグ効果と呼ばれています。
最近ではこれに加えて、がん遺伝子の活性化、もしくは、がん抑制遺伝子の欠落がもたらす特異な代謝経路が次々と報告されており、抗がん剤の標的として代謝酵素が注目されています。
ペントースリン酸経路は、核酸の合成に必須の代謝経路であるにも関わらず、がん細胞におけるその促進機構は不明でした。
本研究成果は、その直接の活性化因子がNrf2であることを明らかにしたものです。
また、
酸化ストレス応答を担うはずのNrf2 が、細胞の増殖刺激存在下において、代謝経路の改変をもたらして増殖を促進するという、がん細胞の悪性化機構の新しい局面が明らかになりました。
さらに、Nrf2 の機能亢進と増殖シグナルとの間に存在する正のフィードバックの発見は、Nrf2 を高発現するがんに対する、より効果的な治療戦略の開発に道を拓くものです。
がん細胞において特異的にNrf2の機能を阻害することは、がんの治療にきわめて有効であると期待されます。
しかし、Nrf2は細胞の内外からの親電子性毒物や活性酸素種などに対する防御機構における鍵タンパク質であることを考えると、Nrf2阻害剤の全身への投与は正常な細胞におけるNrf2の機能抑制をもたらし、薬剤や放射線による副作用を悪化させることが危惧されます。
この研究から、がん細胞の悪性化をもたらすNrf2活性のレベルは、生体防御機能を発揮するのに必要なNrf2活性のレベルをはるかにうわまわっていることが確認されました。
がん細胞においてより効果的に作用するNrf2阻害剤の開発にあたり、こうしたNrf2活性のレベルの違いは有効な手がかりになるものと期待されます。
一方、Nrf2は核に局在するタンパク質であることから創薬の標的としては難易度が高いとされており、Nrf2阻害剤の開発はほとんど進んでいません。
発がん(癌)の原因はなにか?
がんのイニシエーター 慢性炎症

