皆様は免疫チェックポイント阻害剤という薬をご存知でしょうか。
簡単に説明しますと
免疫チェック阻害剤とは、がん細胞の持つ免疫からの攻撃に対する防衛機能を阻害して免疫機能でがん細胞を殺すための薬です。
少し前までの日本では、がんを患った患者は基本的に
手術による治療が治療の中心にありました。
ですが、近年になって
化学療法や放射線療法は著しい進歩が見られ、現在では、抗がん剤や放射線による治療も状況次第では、手術と変わらない効果があると認められています。
これにより、科学療法と放射線療法は手術に続き、がん治療の中心的な治療方法として取り入れられるようになり、患者は基本的にこの3種類の治療方法(
がんの三大療法)のどれかを選択することになったのです。
この、がん治療の中心になっていた3種の治療法に加え、近年
第4の治療方法として注目を集めている治療法が免疫チェックポイント阻害剤などを使用する免疫療法です。
最近では最近ではがんに対して効果があると新聞やニュースなどでも取り上げられるようになった免疫チェックポイント阻害剤ですが、それらの媒体だけではこの治療法を正しく理解することは難しいと思います。
こちらのページでは療法に興味をお持ちの方に
免疫チェックポイント阻害剤の作用順序から療法に関するメリットや費用、そしてテレビや新聞などでは取り上げられることの少ないデメリットのような役立つ情報を提供いたします。
説明していきます。
人体には体内に病原菌や毒素その他の異物が侵入しても、それらに抵抗して打ちかつ能力や異物と反応する抗体を作って発病をおさえる抵抗力を持っており、これを
免疫と呼びます。
生体は自分と同じものである「自己」と異なるものである「非自己」として区別しており、
自身である「自己」に関しては異常が認められない限りは免疫寛容として攻撃をしません。
そして、
自分ではない「非自己」が体内に侵入してきた場合には、それに反応し排除しようとするのです。
この
排除の対象となる「非自己」を抗原と呼び、抗原を排除しようとする生体の働きを免疫応答と呼びます。
また、
生体を病気から保護する体内の機構の総称を免疫系、免疫機構と呼びます。
免疫機構はウィルスや病原菌など身体に害である異物から身を守るために常に準備をしていますが、では免疫反応をひたすらに強化すればいいのかといえばそうではございません。
それは、増大しすぎた免疫機能が過剰反応を起こせば、体内の正常な細胞まで攻撃をし始め、
間質性肺炎や甲状腺機能障害、各種臓器不全などの重篤な副作用が発生する原因にもなるからです。
そのため、
免疫の活動に対してブレーキ役、バランスを調整するためのメカニズムが必要となってくるのです。
免疫チェックポイント分子であるPD-1は免疫機能を調整を担う分子の一つです。
免疫チェックポイント分子はがんの免疫療法に対して深く関与しており、特定の免疫チェックポイント分子に作用することで免疫によってがんの排除を狙うのが免疫チェックポイント阻害剤を利用した治療方法です。
免疫チェックポイント阻害が話題にされる以前でも、免疫機能を強化するなどしてがん細胞に攻撃させることを狙った治療方法はありましたが、十分な効果を発揮できてはいませんでした。
様々な研究の結果、その理由としてポイントとなるのが、がん細胞が元々「自己」である正常細胞が悪性化することで発生していることです。
本来、免疫機能のバランスをとるための免疫チェックポイント分子ですが、これをがん細胞は利用して
局所的な免疫抑制環境を作り出し、免疫機構ががん細胞を攻撃しないようにしていることが分かったのです。
この様な、
がん細胞が持っている免疫細胞の働きを回避する仕組みを免疫回避機構と呼びます。
つまり、免疫機構ががん細胞を効率よく攻撃するためにはがん細胞の作り出した免疫寛容の状態を破綻させる必要があるのです。
免疫チェック阻害剤を利用した治療は免疫チェックポイント分子に作用することでがん細胞の持つ免疫回避機構の働きを阻害します。
これにより、免疫機構はがん細胞を正しく異常細胞として認識できるようになり免疫によるがん細胞の排除が見込めるようになるのです。
免疫抑制サイトカイン |
免疫チェックポイントたんぱく質 |
生理機能脂質 |
|
マイクロRNA遺伝子
IL-6
IL-10
VEGF
TGF-β
ケモカイン
|
CTLA-4
PD-1
TIM-3
LAG-3
B7-H3
B7-H4
B7-H5
TIGIT
|
プロスタグランジンE2
|
これ以外にも癌細胞の周囲やリンパ節や末梢血などに下記のような免疫抑制性細胞が作用することで、がんの免疫抑制環境が構築されます。
・制御性T 細胞(Treg)
・骨髄由来免疫抑制細胞(MDSC)
・腫瘍浸潤マクロファージ(M2型)
・浸潤樹状細胞
●現在承認されている免疫チェックポイント阻害剤(2017年3月時点)
現在、臨床試験が進んでいる免疫チェックポイント阻害薬には3種類ございます。
そのうち2つは
抗PD-1抗体と
抗PD-L1抗体で、これらはそれぞれ
PD-L1と
PD-1と結合することで免疫抑制環境を壊して免疫のがん細胞への攻撃を促します。
残る1つが
抗CTLA-4抗体と呼ばれる薬剤です。
CTLA-4と樹状細胞であるB7が結合することで免疫が非活性化するので、これの結合を妨害することでがん細胞を殺すように働きかけます。
現在、販売されている阻害剤は抗PD-1抗体と抗CTLA-4抗体の2種類です。
抗PD-1抗体 |
製品名 |
承認対象疾患 |
|
二ボルバム
|
オプジーボ
|
メラノーマ
非小細胞肺癌
腎細胞癌
ホジキンリンパ腫
頭頚部癌
|
|
ペムブロリズマブ
|
キイトルーダ
|
メラノーマ
非小細胞肺癌
|
抗PD-L1抗体 |
製品名 |
承認対象疾患 |
|
アテゾリズマブ
|
---
|
非小細胞肺癌
|
|
アベルマブ
|
バベンシボ
|
メルケル細胞癌
|
|
デュルバルマブ
|
---
|
非小細胞肺癌申請中
|
|
抗CTLA-4
モノクローナル抗体
|
製品名 |
承認対象疾患 |
|
イピリムマブ
|
ヤーボイ
|
メラノーマ
|
|
トレメリムマブ
|
---
|
悪性中皮腫
フェーズⅠ治験中
|
抗CTLA-4と抗PD-1の2剤併用使用は、現在治験中です。
抗CTLA-4抗体イピリムマブは、免疫チェックポイントたんぱく質であるCTLAの働きを阻害する、免疫チェックポイント阻害剤として代表される薬品の一つです。
CTLA-4は活性化したCTL細胞(細胞傷害性T細胞・キラーT細胞)に発現する免疫チェックポイント分子です。
CTLA-4分子は、免疫を抑制する機能をもつ物質で、制御性T細胞(Treg)の表面にも存在していて、制御性T細胞の免疫抑制作用のひとつを担っています。
CTL細胞は他の免疫細胞と比べて強くがんを攻撃する特徴がありますが、CTL細胞が体内の異物を効率よく攻撃するためには、他の免疫細胞である
樹状細胞やマクロファージとの協力が不可欠です。
マクロファージは体内の異物を取り込むことで破壊して
サイトカインと呼ばれる、受け取った物質を活性化させる物質を放出させます。
サイトカインはマクロファージが捕食した体内の異物についての情報が詰まっており、対象の異物を集中的に攻撃するよう、免疫機能に指示を出す働きがあります。
樹状細胞も同じように体内の異物を取り込み、破壊します。
異物を破壊した樹状細胞は同様の異物に対策ができるように周囲の免疫細胞に情報を伝達する役割をもっています。
この情報伝達はCTL細胞に対して、特に強く働くのでマクロファージよりも樹状細胞の方がCTL細胞を効率よく活性化させることが出来るといえます。
がん細胞に対しても樹状細胞やマクロファージは食べることで攻撃を行いますが、がん細胞を食べてしまった場合には、これらは
CD80,CD86(B7-1,2)と呼ばれる分子が発現します。
このB7と呼ばれる分子はCTL細胞に発現したCTLA-4と結合することで免疫抑制環境を構築してしまうのです。
つまり、
CTL細胞が効率よくがん細胞を攻撃するためにはCTLA-4分子とB7分子との結合を阻害する必要があるのです。
免疫チェックポイント阻害剤のひとつである
抗CTLA-4抗体イピリムマブはリンパ節の中でCTLA-4分子とあらかじめ結合することでB7分子との結合を妨害して、免疫抑制環境を作成を妨害します。
これにより、癌細胞への攻撃態勢を整えたCTL細胞が、癌のあるそれぞれの部位に移動して、抑制されることなく癌細胞への攻撃をすることができるのです。
抗CTLA-4抗体イピリムマブによる抗腫瘍免疫応答の増強
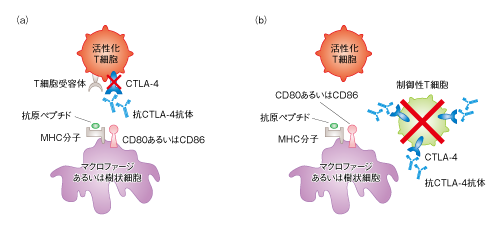 図(a)は活性化T細胞に発現したCTLA-4に対する抗CTLA-4抗体の作用を示しています。
図(a)は活性化T細胞に発現したCTLA-4に対する抗CTLA-4抗体の作用を示しています。
CTLA-4と抗CTLA-4抗体が結合することでB7(CD80,CD86)に結合することで発生する免疫抑制環境を解除します。
図(b)は制御性T細胞に発現しているCTLA-4に対する抗CTLA-4抗体の作用を示しています。
活性化T細胞とは違い、制御性T細胞は恒常的にCTLA-4を発現しています。
CTLA-4と結合した抗CTLA-4抗体を介した結果、産生される抗体には、制御性T細胞を除去する作用があり、これにより制御性T細胞による免疫抑制環境も解除します。
イピリムマブの臨床結果
実際にがん患者にイピリムマブを服用した際の結果について解説します。
【対象】
メラノーマを患っており、切除が不能な治療歴長い欧米人患者676人
※メラノーマ:皮膚細胞の中の基底層にある「色素細胞」ががん化したもの、悪性黒色腫とも呼ばれる非常に悪性度の高い皮膚がん
2015年7月に、抗CTLA-4抗体イピリムマブは「根治切除不能な悪性黒色腫(メラノーマ)」に対する効能、効果を認められて製造が承認されました。
【内容】
患者を無作為に3:1:1の割合で3グループに分割
グループA:イピリムマブ3mg/kgとペプチドワクチンgp100を併用使用(403人)
グループB:イピリムマブ3mg/kgのみを投与(137人)
グループC:ペプチドワクチgp100のみを投与(136人)
【評価項目】
各グループを生存期間(os)の中央値と生存率ついて比較検証した。
|
生存期間の差異(中央値)
|
|
グループA:10.0ヶ月
グループB:10.1ヶ月
グループC: 6.4ヶ月
|
|
1年生存率
|
|
グループA:43.6%
グループB:45.6%
グループC:25.3%
|
|
2年生存率
|
|
グループA:21.6%
グループB:23.5%
グループC:13.7%
|
※グループA、Bの3年生存率は約22%程で以降の生存率はほぼ一定となり長期生存が確認されています。
イピリムマブによる治療の副作用
上記の実験からイピリムマブには進行がんに対する延命効果が認められたが、同時に
T細胞の過剰な活性化と増殖により、重度の免疫関連の有害事象を引き起こす危険性があります。
※有害事象とは投薬などの治療によって生じた、あらゆる好ましくない症状や徴候のことを指します。この際に治療と症状との因果関係は問いません。
|
イピリムマブにより発現する主な有害事象(副作用)
|
|
皮膚
|
皮膚炎、そう痒症
|
|
消化管
|
下痢、大腸炎
|
|
肝臓
|
肝機能値異常、肝炎
|
|
内分泌腺
|
下垂体炎、副腎異常、甲状腺異常
|
|
神経系
|
末梢性ニューロパチー
|
|
その他の臓器
|
間質性肺炎、ブドウ膜炎、上強膜炎、腎炎
|
この有害事象は治療の初期に皮膚や消化管に発現しやすいが、投与中止後、数週間から数カ月を経て発現する場合もあります。
イピリムヤブ由来の有害事象の対応策
・副作用が発現した際には速やかにステロイドによる治療を開始します
・症状が回復した場合にも再発を避けるためにステロイドを少しずつ漸減することが大切です
・これによる改善が認められない場合には、他の免疫抑制剤を投与して経過を確認します
有害事象を評価する際は、その重症度を1~5段階の
Gradeに表します。
|
有害事象の評価基準
|
|
Grade1:軽症
Grade2:中等症
Grade3:重症または医学的に重大ではあるが、ただちに命を脅かすものではない
Grade4:症状によって命が脅かされている
Grade5:有害事象による死亡
|
|
Grade3以上の有害事象を発現した比率
|
|
グループA:10~15%
グループB:10~15%
グループC: 3%
|
|
同実験中の試験治療薬に関連した死亡率
|
|
2.1%(676人中14人)※
|
※うち半数は免疫に関連した有害事象によるもの
【総括】
・イピリムマブを投与したグループAとグループBは生存期間の延長、生存率の向上が見られた
・ペプチドワクチンと併用使用した場合と単独使用した場合に評価項目に対する差異は認められなかった
・イピリムマブを投与したグループAとグループBはGrade3以上の重篤な有害事象を発現する比率が向上した
※本薬副作用の補足
欧米人と日本人とでは、体質が異なる為、副作用の出方が異なる場合がある事を考慮する必要があります。
イピリムマブは国内臨床試験では、副作用が軽度のなものを含めて
81.0%確認されています。
|
国内で確認されたイピリムマブの副作用
|
|
倦怠感(11.9%)
そう痒感・斑状丘疹状皮疹(各14.3%)
間質性肺疾患、大腸炎、重度の下痢、皮膚粘膜眼症候群、多形紅斑、類天疱瘡、神経障害、肝機能障害、肝炎、甲状腺機能障害、下垂体機能障害、腎障害、膵炎、筋炎、横紋筋融解症、重症筋無力症、脳炎、髄膜炎、Infusion、※1型糖尿病
|
※1型糖尿病に関しては類薬である
ニボルマブに発症報告があることから本薬使用においても同様の副作用が起こりうる為に、既に注意喚起が行われています。
イピリムマブの費用
治療開始から1ヵ月間の治療費(薬剤費と医療費)
全額自己負担の場合
351万9690円
混合診療(保険外併用療養)が認められた場合
341万2470円
イピリムマブの類似薬であり免疫チェックポイント阻害剤のひとつである
トレメリムマブは
イピリムマブと同じく、CTLA-4の活性化を阻害することで、がんの免疫抑制環境の構築を妨害します。
海外では、悪性中皮腫患者に対する後期第2相臨床試験を実施中で、2015年に
米国食品医薬品局から悪性中皮腫の治療薬候補として希少薬の指定を受けました。
※悪性中皮腫:主な発現箇所が胸部および腹部の内膜(胸膜、腹膜)である希少かつ悪性度の高いがんです。
悪性中皮腫は
アスベスト(石綿:せきめん・いしわた)を吸うが主な発現原因であるとされ、症状が進行した際は有効な治療方法が少なく、治療を行っても5年生存率が5%未満という非常に恐ろしいがんです。
日本では2014年5月より一般的な固形がんを対象として臨床実験が行われていましたが、悪性中皮腫治療のアンメットニーズ(新たなニーズ)に対応するために2015年10月より日本の悪性中皮腫患者を対象として国内での相臨床試験を開始しました。
※アストラゼネカプレスリリースから画像転載
臨床試験情報(JAPIC-CTI)
抗PD-1抗体二ボルバムは、免疫チェックポイントたんぱく質であるPD-1の働きを阻害する、免疫チェックポイント阻害剤として代表される薬品の一つです。
PD-1(programmed cell death 1)は活性化したT細胞の細胞死誘導時に表面に発現が増強される遺伝子です。
一方でPD-1と対になるPD-L1とPD-L2は通常抗原提示細胞(樹状細胞、マクロファージ)の表面上に発現します。
この
PD-1とPD-L1が結合することでT細胞からのサイトカインの産生を減少させるシグナルを発生させ、T細胞の活動を抑制して免疫抑制環境を構築します。
この反応は本来、必要な場合のみ発動し、免疫の攻撃能力を調整することで自己免疫疾患となることを防いでいます。
ですが、この
PD-L1は腫瘍細胞や腫瘍微小環境に存在する非形質転換細胞の細胞表面上にも強く発現しています。
この為、排除するべき腫瘍細胞に対してもT細胞の活動の抑制が起こり、免疫による除去が行えないのです。
このPD-1とPD-L1及びPD-L2の結合を
PD-1に結合することで妨害して、免疫抑制環境の構築を妨害する為の抗体が免疫チェックポイント阻害剤である抗PD-1抗体
二ボルバムです。
抗PD-1抗体 二ボルバムの作用
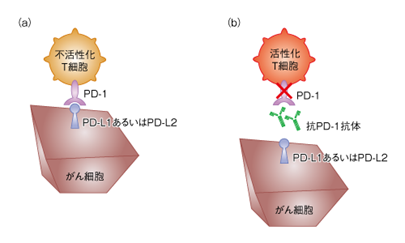
・図(a)では活性化T細胞の表面に発現するPD-1と癌細胞に発現するPD-L1あるいはPD-L2が結合することで、免疫抑制環境が構築されてしまうので免疫はがん細胞への攻撃を行うことができません。
・図(b)では結合を行う前に抗PD-1抗体が先んじてPD-1に結合します、これによりPD-L1は結合先を失い、免疫抑制環境の構築されないので免疫はがん細胞を活発に攻撃することができます。
二ボルバムの臨床効果
日本ではニボルバムの効果は悪性黒色腫(メラノーマ)に対して高い奏功率を認められ、2014年にがんに対して有効な治療薬として承認されました。
ニボルバムの臨床試験結果(欧米)
有効性が認められた |
高い効果が見られた |
|
・非小細胞肺癌
・前立腺癌
・大腸癌
・腎細胞癌
|
・悪性黒色腫(メラノーマ)
・腎細胞癌
|
※特にメラノーマ29%や腎細胞癌では13%の奏効率が報告されました
進行期非小細胞肺癌(扁平上皮癌)では、プラチナ製剤を含む化学療法歴を有する患者に対する二次治療として、転移・再発乳がんや進行肺がんの標準治療薬の1つである
ドセタキセルを上回る有効性が示されました。
二ボルバムの副作用
大腸炎、肺炎、甲状腺炎、下垂体炎、皮膚炎、Ⅰ型糖尿病、筋炎、末梢神経炎、重症筋無力症等があり、死亡例も報告されています。
二ボルバムの薬剤費用
20㎎ :約15万円
100㎎ :約73万円
例)体重60㎏の方の1年約52週とした場合
悪性黒色腫(メラノーマ):約1523万円
非小細胞肺癌:約2288万円
※治療費は含まず、全額自己負担の場合
抗PD-1抗体二ボルバムと抗CTLA-4抗体イピリムマブの二剤併用療法
最新の研究結果ではオプジーボR(一般名:ニボルマブ)とヤーボイR(一般名:イピリムマブ)の併用療法が未治療の進行期非小細胞肺がんにおいて臨床的に意義のある奏効を示しました。
参考資料
一部の薬剤が事前検査にて奏功(効果の有無)の判断が可能となりました
免疫チェックポイント阻害剤を使用した治療方法はまだまだ研究段階です。
最近でも、ある種の薬品と組み合わせることで効果の増強が確認されるなど様々が発見がされています。
今回、注目を集めたのは
PD-1阻害剤であるペンブロリズマブの効果量をミスマッチ修復遺伝子と呼ばれる遺伝子を確認することで投薬前に予測できるという発見です。
ミスマッチ修復遺伝子とはDNA複製や遺伝的組換え時に生じる核酸塩基の損傷を治すためのDNA修復システムの1つです。
38名の進行したがん患者に対してミスマッチ遺伝子の状態に注目して免疫チェックポイント阻害剤(ペンブロリズマブ)を投与したところ以下のような結果が見られた。
|
ミスマッチ修復遺伝子に欠陥のあった大腸がん患者計13名
|
|
|
|
|
|
|
|
|
|
|
ミスマッチ修復遺伝子に欠陥のなかった大腸がん患者患者計25名
|
|
|
この結果から
ペンブロリズマブが大腸がん細胞に対して有効な作用するにはミスマッチ遺伝子に欠陥があることが必要な可能性が高いことが推測されています。
既にミスマッチ修復の欠陥の有無は検査可能なため、免疫療法の効果量に対する目印になるのではないかと期待され、更なる研究が進められています。
|
ミスマッチ修復遺伝子に欠陥のあった大腸以外のがん患者計10名
|
|
|
|
|
|
|
|
|
|
|
|
|
ニボルマブ(オプジーボ)の効果を増強する薬剤を発見
免疫チェックポイント阻害剤のひとつである
抗PD-1抗体二ボルバム(オプジーボ)の効果が高脂血症の治療に用いられるベザフィブラートと併用した際に増強されることが京都大の本庶佑客員教授と茶本健司医学研究科講師らの実験によって分かりました。
実験では、ベザフィブラートだけの投与ではがんに対して大きな効果はなかったが、
免疫チェックポイント阻害剤と併用した際にがんの治療効果が大幅に高まることを確認されました。
ベザフィブラートには活性化することで免疫力の向上作用を与えるミトコンドリアの活動を促進作用があります。
これを免疫チェックポイント阻害剤と組み合わせることで今まで
全体の3割~5割程度を占めていた免疫チェックポイント阻害剤を用いた治療に対して反応のない、もしくは殆どないがん患者にも療法を効果的に作用させることが出来る可能性が出てきたのです。
現在は動物実験の段階ですが、オプジーボとの併用治療を行う治験は、肺がんの患者を対象に来年度にも行われる予定です。(2017年1月現在)
免疫チェックポイント阻害剤による治療はいままでの抗がん剤による治療とは全く異なるメカニズムで作用しております。
抗がん剤は投与することでがん細胞を破壊しますが、
この作用は活発に動いている細胞に対して無差別に効果を発揮しますので、
、
がん細胞だけではなく正常な細胞群にも攻撃を行います。
このため患者による治療効果の差が非常に大きく、現れる副作用の種類も数多くあるのです。
免疫チェックポイント阻害剤による治療は抗がん剤の無差別な攻撃とは異なり、
がんの免疫抑制環境を構成するための細胞だけに狙いを絞って作用します。
これによって、
癌の免疫回避機構の働きを阻害し、免疫が癌細胞を攻撃できるように仕向けます。
この無差別ではなく特定の細胞にアプローチするがん治療方法は画期的といえ、研究が進むことでがんの根本的な根絶が実現させる可能性も秘めています。
この為、現在でも様々な研究機関でも日々研究が行われており、免疫チェックポイント分子に対して様々な影響を与える薬剤が開発されています。
ですが、免疫チェックポイント阻害剤に興味を持った方々には注意してもらいたいことがあります。
それは、免疫チェックポイント阻害剤によるがん治療の研究は新しいからこそデータが少なく、未だに研究されている段階であるということです。
研究段階であるということは治験によるデータ収集が少なく、効能に関しても科学的根拠に乏しいといったものが含まれているかもしれないという意識が必要になります。
少し前では、TVや雑誌などでは主に「抗PD-1抗体オプジーボ」について、がんの治る夢の新薬、副作用のない奇跡の薬といった過剰な評価をされた情報が散見されていました。
これらの情報を鵜呑みにしてしまった患者は副作用がないもしくは少ないという意識から、安易に治療方法を試しました。
その結果、自己免疫疾患などの重篤な副作用がでてしまったり、曖昧な治療方針から症状が悪化し死亡する場合もあったのです。
勘違いしないでもらいたいことは、だからといってオプジーボを使用した
免疫療法が行ってはいけない欠陥のある治療ではないということです。
現在でも欧米では様々な条件で治験が行われており、延命困難な患者に対して何ケ月かの間SD(不変)状態の維持効果や腫瘍縮小効果が確認されています。
日本での治験は欧米と比べ、まだ数が少なく、日本人に最適な治療方針が固まっているとはいえません。
例え、欧米で効果のあった方法をそのまま実行しても、生活習慣や人種などの違いによって日本では異なる治験結果が現れてしまうのです。
下記に乗せた例ではオプシーボと他の免疫療法を組み合わせた治療を行った結果、自己免疫疾患、多臓器不全、それらによる死亡するという医療事故が起こりました。
この事故は治療に関する情報不足から免疫のブレーキ機能を弱めたまま免疫機能を過剰に向上させるような、本来は同時に行ってはいけない治療方法を同時に行ってしまった結果です。
そもそも免疫チェックポイント阻害剤はがんを攻撃するために免疫のブレーキ機能を解除してしまう薬です。
この
免疫のブレーキ機能は本来、人体を守るために必要な機能の一つです。
これが機能しなくなってしまうと人体の正常な細胞まで免疫が攻撃してしまう自己免疫疾患という病気になってしまいます。
つまり、ひたすらにブレーキ機能を弱くすればいいのではなくがんを攻撃するように仕向けたまま正常細胞を攻撃しない非常に繊細なバランスが求められるのです。
新薬はよい部分だけ並べられて、悪い部分の情報が入手しにくくなる傾向があります。
だからこそ新しい治療方法ほどメリットだけではなくデメリットを十分に理解する努力を医師だけではなく患者側も行い、実際に療法を行うかどうかを判断する必要があるのです。
オプジーボは夢の新薬ではないので、投薬による効果が無いことも珍しくなく、副作用も自己免疫疾患などの完治の見込めない重篤なものです。
ですが、これらのリスクを認識したうえで
適切な治療を行うのであれば十分な延命効果の見込める効果が見込める療法なのです。
患者の皆様には自身の行う治療方法に関して後悔をしないためにも
インフォームド・コンセントや
セカンドオピニオンを通して十分に理解してから治療を行う必要があるといえるでしょう。
※インフォームド・コンセント:
医療行為を行う際に治療内容についてよく説明を受け十分理解した上で患者の意志に基づいて治療方法を決めること
対象となる療法の目的、方法、効果、予後を含めた副作用の有無や内容などの詳しい情報を得る機会となります
※セカンドオピニオン:
インフォームド・コンセントなどで主治医から得た情報以外にも別の医師の意見を求めること
医療について詳しくない多くの患者は、医師から得た情報から治療方法を選択することになります
この際に、主治医以外の医師からも情報を得ることで、患者側が多くの情報を得て、自身の納得のいく治療を選択する機会が生まれます
オプシーボに関する情報
オプシーボ免疫療法と併用で男性死亡
がん治療薬「オプジーボ」を使用後に、別のがん免疫療法を受けた60代男性が、副作用とみられる症状で死亡したとして、オプジーボを製造する小野薬品工業(大阪市)は19日、こうした治療を同時に行わないよう医師らに注意を呼び掛けた。
小野薬品によると、男性は肺がんで、オプジーボの投与から約3週間後に、自身から取り出した免疫細胞を活発にして体内に戻すがん免疫療法を自由診療で実施したとみられる。その後、多臓器不全となり心不全で死亡したという。
このほかにも5人に、がん免疫療法との併用で重い副作用が出たとの報告があった。
安全性・適正使用情報
※オプジーボ.jp 小野薬品工業株式会社へ飛びます
2014年7月から2017年1月までに
オプシーボ免疫療法を行ったメラノーマ、非小細胞肺がん、腎細胞がんの副作用が出た患者数は7568人、重篤な副作用が発生した患者数は2479人で副作用の起こった患者の約32.8%でした。
オプシーボはオプシーボ(二ボルバム)悪性リンパ腫(非ホジキンリンパ腫)に適用拡大され、2017年2月より薬価が、正式に50%(現:100mg1瓶36万4925円)引き下げられました。
副作用の少ない安全な治療法といわれてきましたが、免疫チェックポイント阻害剤の研究は未だに未知の部分も多く、副作用が少ないとはいえません。
オプシーボで起こりうる副作用には難治疾患も含まれていますので治療を始める前に十分検討する事をお勧めいたします。
・がん免疫応答抑制ネットワークと免疫チェックポイント阻害薬 国立がん研究センター先端医療開発センター 免疫TR分野
・Neutralizing tumor acidic environment improves immune-targeting therapies March 17, 2016 Cancer Research Moffitt Cancer Center
・がん免疫療法とPD-1/PDL1チェックポイント・シグナル伝達 Abcam
・がん細胞が免疫から逃れるメカニズムの解明-免疫チェックポイント阻害剤の効果予測への応用に期待 京都大学医学研究科腫瘍生物学、東京大学医科学研究所附属ヒトゲノム解析センター、 北海道大学大学院医学研究科免疫学、共同研究 2016年5月23日付で英国の科学誌「Nature」電子版にて公開
・がん免疫療法:基礎研究から臨床応用にむけて 2015年4月21日 杉山大介・西川博嘉 (国立がん研究センター先端医療開発センター 免疫TR分野)
・脚光を浴びる新たな「がん免疫療法」:小野薬品のオプジーボ nippon.com
・オプジーボ.jp 小野薬品工業株式会社から転載
・抗PD-1抗体が治療歴のあるメラノーマ,非小細胞肺がん,腎細胞がんで腫瘍縮小効果を示すAnti-PD-1 (BMS-936558, MDX-1106) in patients with advanced solid tumors: clinical activity, safety, and a potential biomarker of response MediEigo
・抗 CTLA-4 抗体イピリムマブ(ヤーボイR)の特性と副作用への対応について 日本皮膚科学会悪性黒色腫の新薬に関する安全性検討委員会
・PD-1とLAG-3は協調して自己免疫の発症を制御する 科学技術振興機構(JST)イノベーション推進本部 研究領域総合運営部 徳島大学疾患ゲノム研究センター
・二ボルマブ(遺伝子組換え)の「使用上の注意」の改訂について 独立行政法人 医薬品医療機器総合機構
・免疫チェックポイント阻害剤の効く人に一つの特徴、「ミスマッチ修復遺伝子」の欠如が左右 米国ジョンズ ・ ホプキンス大学研究グループが2015米国臨床腫瘍学会年次総会で発表されると共に、オンライン 5 月 30 日ニュー イングランドの医療ジャーナル・オブ・メディシン誌から掲載

